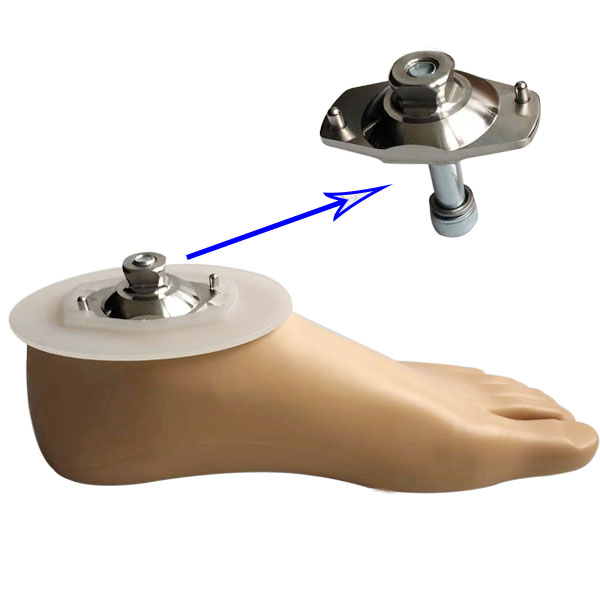
新しいスタイルの工場直送人工義肢部品サックフットアダプター
新しいスタイルの工場直送人工義肢部品サックフットアダプター
| 商品名 | 新しいスタイルのすべてのCNCサックフットアダプター |
| 商品番号。 | 2R8=M10 |
| 色 | 銀 |
| 素材 | ステンレス鋼 |
| 製品重量 | 130g |
| 体重まで | 100kg |
| 使用する | 義肢の下肢部品への使用 |
会社概要
.業種 : 製造業者および貿易業者
・主な製品:義肢部品、装具部品
.経験:15年以上。
.マネジメントシステム:ISO 13485
.場所:石家荘、河北省、中国。
- 処理手順:
図面設計 - 金型製作 - 精密鋳造 - CNC 機械加工 - 研磨 - 表面仕上げ - 組立 - 品質検査 - 梱包 - 在庫 - 配送
- 証明書 :
ISO 13485/ CE/ SGS MEDICAL I/II 製造証明書
- アプリケーション:
プロテーゼ用;装具用;対麻痺の場合;AFO ブレースの場合。KAFOブレース用
- お支払いと配送
.支払方法:T/T、ウエスタンユニオン、L/C
.Delivery Tiem: 支払いを受け取った後 3-5 日以内。
㈠クリーニング
⒈ 湿らせた柔らかい布で製品を拭いてください。
⒉ 柔らかい布で製品を乾かしてください。
⒊ 残留水分を除去するために自然乾燥させます。
㈡メンテナンス
⒈プロテーゼ コンポーネントの目視検査と機能テストは、使用開始から 30 日後に実施する必要があります。
⒉通常の診察時にプロテーゼ全体の摩耗を検査します。
⒊年次安全点検を実施する。
注意
メンテナンスの指示に従わなかった
機能の変更または損失、および製品の損傷による怪我の危険性
⒈ 以下のメンテナンス指示に従ってください。
㈢責任
メーカーは、本書に記載されている説明と指示に従って製品を使用した場合にのみ、責任を負います。メーカーは、本書の情報を無視したこと、特に不適切な使用または許可されていない変更が原因で生じた損害について責任を負いません。製品。
㈣CE適合性
この製品は、医療機器に関する欧州指令 93/42/EEC の要件を満たしています。この製品は、指令の附属書 IX に概説されている分類基準に従って、クラス I デバイスとして分類されています。したがって、適合宣言は、指令の附属書 VLL に従って、製造業者が単独で責任を負います。
㈤保証
メーカーは、購入日からこのデバイスを保証します。保証は、材料、製造、または構造の欠陥の直接の結果であることが証明され、保証期間内にメーカーに報告された欠陥を対象としています。
保証条件に関する詳細情報は、有能なメーカー販売会社から入手できます。